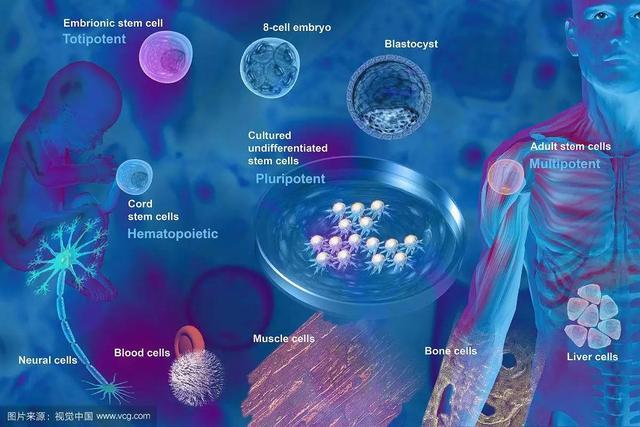
在2020中国生物技术创新大会上,专家指出,干细胞作为战略资源具有战略性、公益性和支持性,其中战略性是面向国家安全和未来竞争,公益性是面向人口健康与社会发展,支持性是面向科技、产业和经济发展。实现干细胞战略资源的收集、储存、开发、利用和共享,推进临床转化,是保障人民健康的重要举措。
干细胞资源是国家重要的战略资源,如何安全有效的保存我国特殊、唯一、稀有的人类生物资源,对促进我国人口健康、维护生命资源安全、治疗重大疾病等具有重要的意义。
干细胞的重要价值体现之一是在疾病治疗中的应用。
诺贝尔生理学或医学奖获得者Thomas C. Sudhof教授曾表示, “我们可以把疾病进行控制,干细胞是一个非常好的治疗方法”。在传统医学治疗无法解决的问题上,干细胞研究将带来新的希望。”
国际上美国、韩国、日本、欧盟等均已有经批准的干细胞治疗产品上市,干细胞治疗疾病正成为更为广泛的现实。
截止2021年4月,在ClinicalTrials.gov网站检索到的间充质干细胞临床试验超过1200个。
近年来,这个数字持续增长,表明间充质干细胞的重要性日益增强。
目前,我国的干细胞药物研发愈发规范,吸引大量资本和人才进入。值此成果即将井喷之际,我们通过梳理国外间充质干细胞药物,来展望这一市场。
据不完全统计,全球曾经获准上市的间充质干细胞产品有18款,符合药品定义的有10款。
18款间充质干细胞相关产品(含孤儿药、有条件批准药品、医疗产品等);批准日期和国家为首次批准;Multistem未统计,因其官网称该药不是间充质干细胞
01
多点开花,Mesoblast
Prochymal:移植物抗宿主病
国家:美国、加拿大、新西兰
日期:2010-05
细胞类型:骨髓间充质干细胞
适应症:移植物抗宿主病、克罗恩病
价格:20万美元/疗程
最初,美国FDA以孤儿药的方式批准其用于I型糖尿病的治疗。
2012年,Prochymal被卖给澳大利亚的Mesoblast,并在加拿大、新西兰获批上市,治疗急性移植物抗宿主病。
2015年,Mesoblast与JCR合作,将其改名Temcell在日本上市。
Temcell:移植物抗宿主病
国家:日本
日期:2016-02
细胞类型:骨髓间充质干细胞
适应症:移植物抗宿主病
价格:约12万美元/系列疗程
如前所述,Temcell前身是Osiris公司的Prochymal,Mesoblast公司的Ryoncil。
2019年,TEMCELL又被批准治疗大疱性表皮松懈症和新生儿缺氧缺血性脑病。
在JCR的财报中,Temcell的销售收入在2018年约1800万美元,2019年约2800万美元。
MPC:骨修复
国家:澳大利亚
日期:2010-07
细胞类型:自体间质前体细胞
适应症:骨修复
价格:未知
2010年,Mesoblast自主研发的MPC(Mesenchymal Precursor Cell)在澳大利亚获得批准上市,用于受损组织的修复和再生。
Mesoblast目前市值约10亿美元,2020财年660万美元商业收入全部来自Temcell,主要收入来自中国、日本等合作方的里程碑付款(2500万美元)。
02
先行先试,韩国FDA
CellGram:急性心肌梗死
国家:韩国
日期:2011-07
细胞类型:自体骨髓间充质干细胞
适应症:急性心肌梗死
价格:1.5万美元
CellGram在胸绞痛发生后72小时内,通过冠状动脉成形术使用,以改善心肌梗死患者的左心室血细胞计数。在治疗6个月后测量显示,每一次治疗提高了6%的左心室射血分数。
到2017年,这种疗法已经创造了约780万美元的销售额。但CellGram在6年期限内未能满足治疗600名患者的条件,Pharmicell公司申请将患者最低数量要求降低到60人,遭到拒绝。
一些行业观察家因此猜测韩国会取消其批准,但这是韩国第一个干细胞药,“批准的取消将对国家声誉产生有害影响,我们必须做出谨慎的决定。”
Cartistem:退行性关节炎
国家:韩国
日期:2012-01
细胞类型:脐血间充质干细胞
适应症:退行性关节炎和膝关节软骨损伤
价格:1.9-2.1万美元
在Cartistem上市应用的8年中,累计销售已经超过18000剂。
从2017年到2020年,Cartistem已连续4年销售额超过100亿韩元(约900万美元),这一表现明显优于韩国批准的另外3款干细胞药品(年销售额都不到50亿韩元)。
Medipost季度销售趋势(百万韩元,来源:Medipost)
Kim SJ等研究者对128名产品使用者进行了回顾性分析,结果发现在随访2年后,这些患者的疼痛和功能得到改善,且有统计学意义。
目前,该产品已在美国完成I期和IIa期临床试验,正在日本开展II期临床试验。
Cupistem:克罗恩病
国家:韩国
日期:2012-01
细胞类型:自体脂肪间充质干细胞
适应症:复杂性克罗恩病并发肛瘘
价格:3000-5000美元
Cupistem被用于减轻克罗恩氏瘘管的炎症。
在一项II期临床试验中,43个患者在12个月后评估了瘘管愈合情况,其中80.8%的患者表现为完全的瘘管愈合。24个月后,这些患者中有75%完全闭合,显示出可持续的安全性和治疗效果。
NeuroNATA-R:肌萎缩侧索硬化症
国家:韩国
日期:2014-07
细胞类型:自体骨髓间充质干细胞
适应症:肌萎缩侧索硬化症、运动神经元病
价格:1.8-7.2万美元(根据体重)
NeuroNATA-R是韩国Corestem公司提供的干细胞疗法。在每次注射干细胞的4周前,需要从患者自身的骨髓中采集间充质干细胞。
在评估安全性的I期临床试验中,有7位患者接受了鞘内注射两次,并随访了12个月。该研究显示它有良好的安全性。
03
不甘落后,日本印度
Stempeucel:严重肢体缺血
国家:印度、欧盟批准
日期:2015-06
细胞类型:骨髓间充质干细胞
适应症:血栓闭塞性动脉炎
价格:2200美元(2017)
2015年,Stempeucel以孤儿药的形式获得了欧洲药品管理局(EMA)的批准,治疗血栓闭塞性动脉炎。
2017年,印度药品管理总局(DCGI)授予了Stempeucel有限营销许可,用于治疗因Buerger病引起的严重肢体缺血患者。2020年,DCGI完成了正式批准。
Stempeucel的研发历时12年,最终成为印度第一个被批准用于商业用途的同种异体细胞治疗产品。
Alofisel:克罗恩病
国家:日本、欧盟批准
日期:2018-3
细胞类型:脂肪间充质干细胞
适应症:克罗恩病患者复杂肛周瘘
价格:约7万美元/疗程
2018年,日本制药巨头Takeda与比利时干细胞公司TiGenix联合宣布,EMA已批准Alofisel (darvadstrocel,Cx601),用于瘘管对至少一种传统或生物疗法反应不足的克罗恩病复杂性肛周瘘的治疗。
但Alofisel在获得所谓第三级批准时遇到了一些困难,这是用来指代国家级付款人保险的术语。例如,英国NICE拒绝推荐Alofisel,理由是其在临床试验中获益不大。
2019年,Takeda决定在欧洲采取基于价值的定价。也就是说,如果患者没有改善,他们将承担部分或全部费用。
在截止2020年3月31日的财政年度中,Takeda从Alofisel获得的收入约35万美元。
Stemirac:脊髓损伤
国家:日本
日期:2018-12
细胞类型:自体骨髓间充质干细胞
适应症:脊髓损伤
价格:13.5万美元
Stemirac的上市有些争议,它只做了II期临床试验,就获得了有条件批准,并被纳入国民健康保险。
此举遭到Nature批评,认为其临床试验中没有对照组,治疗组只有13名受试者。而日本方面则回应,设立对照组可能产生道德问题。
据2019年的一篇文章预测,Stemirac将在未来9年中,每年给Nipro公司带来约340万美元的收入。
04
我国干细胞临床治疗步伐加速!
根据国家药品监督管理局药品审评中心的数据,截止目前,我国已经有8款间充质干细胞新药申请获得临床批件,适应症急性移植物抗宿主病、类风湿关节炎、缺血性脑卒中、膝骨关节炎、糖尿病足。
来源:CDE
目前,我国干细胞治疗的监管采用“双轨管理模式”,国家卫健委主要管理由医疗机构开展的临床研究,药监局主要负责按照药物完成临床试验后申请上市的干细胞治疗产品。
近两年,我国干细胞临床应用在“双轨管理模式”下规范化发展,截止目前已经有74个干细胞临床研究项目通过了国家卫健委的备案。连续有8款干细胞新药申请获得了药监局的试验默示许可。
与过去几年相比,我国干细胞临床转化正以全新的趋势在发展,国内干细胞上市药物的空白有望更快得到填补。
当前,在干细胞转化领域,我国的研究主要集中在干细胞库、干细胞药物应用、临床前研究和临床试验等方向。监管政策的逐渐完善将我国干细胞临床转化推向了新的发展局面。
第一,我国进入到了全新的干细胞新药发展阶段。《细胞治疗产品研究与评价技术指导原则(试行)》的颁布明晰了干细胞治疗作为药品申报的标准, 同时“60天临床试验默示许可”的新药审批新制度,给我国干细胞新药的研发和申报提供了新的发展机遇。
第二,国家“干细胞及转化研究”重点专项推动干细胞治疗药物的研制。例如,重点专项申报指南指出的考核目标之一是针对某种重大疾病或罕见病研制细胞治疗药物,申请干细胞新药注册以及申请干细胞临床批件。
第三,政策鼓励综合企业的力量来推动干细胞临床转化。在过去两年里,国内出台的一些政策明文支持有资质的三甲医院与符合条件的社会力量合作申报和开展干细胞临床研究工作,也就是支持和鼓励符合条件的社会力量或制备机构(企业)加入到干细胞行业中来,一起推动干细胞的临床应用与发展。企业创新力量的推动,加快了国内干细胞的研发应用进程。
当前,仍然有很多疾病需要创新疗法来解决未得到满足的临床需求,而干细胞新药扩大适应症正是为了满足这些需求。
05
围产组织干细胞渐渐成主流
围产组织是间充质干细胞的最大来源之一,成为了新药研发备受青睐的干细胞来源。围产组织来源间充质干细胞具有多向分化潜能、免疫学特性、取材方便无危害、来源广泛易于工业化制备等优点,成为了医学发展的新趋势。当前国内获得临床批件的干细胞新药中超过60%采用了围产组织来源的间充质干细胞。
在新冠肺炎重症患者的救治中,围产组织来源间充质干细胞也显示出了很好的疗效。国内的研究报道显示,新冠肺炎危重症患者回输围产组织来源间充质干细胞9天后,转出了ICU病房,大部分生命体征和临床试验指标恢复正常,两次喉部拭子检测均呈新冠病毒阴性。
近年来,源自于围产组织的免疫细胞也渐渐成为了研究热点。此前,美国FDA就批准了人类胎盘干细胞衍生的免疫细胞治疗新冠肺炎的临床试验,这款疗法由美国新泽西州生物技术公司Celularity开发。
在早期试验中,将有多达86名有症状的新冠肺炎患者接受治疗,以评估该疗法的安全性,以及阻止患者病情进一步加重的能力。
国际上,胎盘细胞治疗产品也在加速进入市场的步伐。例如,近年来备受关注的胎盘源贴壁细胞PLX-PAD,正被设计用于治疗无需组织或遗传配型的患者。
该疗法通过了美国和欧盟两个地区的加速审批路径——包括美国FDA的快速审定资质和欧盟EMA的自适应路径计划(Adaptive Pathways program),用于肢体缺血的治疗。此外, PLX-PAD还被应用于其他适应症的临床研究,包括间歇性跛行、骨科适应症、肺动脉高压以及女性健康等,部分已经进入了临床III期。
当前我国干细胞行业已经形成了庞大的市场规模,随着临床转化以及市场的发展,干细胞在国内造福患者的时代也将到来。
来源:https://www.cn-healthcare.com/articlewm/20210715/content-1243437.html
1. 添加医学顾问微信,扫描☟二维码
2. 备注【您想咨询的问题】

我们致力于干细胞科普知识的推广与普及,专注于干细胞最新资讯提供和干细胞治疗专家咨询服务。
免责声明:本站内容仅供参考,不作为诊断及医疗依据