卵巢早衰(POF)又被称为“原发性卵巢功能不全”或“提前绝经”,是指女性40岁之前发生的卵巢功能衰退,以月经稀发或闭经、促性腺激素(Gn)水平升高、雌二醇水平降低为特征,而且会明显降低自然怀孕的可能性。常伴有潮热、盗汗、脱发、皮肤黏膜干燥、xing欲减退等多种围绝经期症状,此类患者患心理障碍、骨质疏松、心血管疾病、认知功能障碍、自身免疫性疾病、泌尿生殖系统感染等疾病的风险也会有所增加。
本病影响着1%~3%成年女性的身心健康,甚至使很多女性失去做妈妈的权利,而且依靠传统的治疗手段尚无法有效恢复患者的生育能力。而随着再生医学的不断发展,干细胞疗法有望让卵巢“回春”,为卵巢早衰患者带来了“送子”的希望。

▲图源“摄图网”
卵巢是女性重要的生殖器官,对性激素产生、调节生殖周期和月经具有至关重要的意义。卵巢的外层包含称为卵泡的独特结构。在女性的生育过程中,原始卵泡的数量是有限的,随着女性年龄的逐渐增大、生理性或病理性原因,会导致卵泡逐渐减少,甚至终止排卵,此时女性就进入了生殖衰老或更年期。而卵泡减少的本质是卵泡耗竭后,内源性卵巢女性生殖系干细胞(FGSCs)数量减少,因此,探索FGSCs衰老的机制,有助于从根本上解决女性卵巢衰老问题。
关于卵巢早衰病因和发病机制较为复杂,目前尚未十分清楚,可能与遗传、X染色体异常、单基因突变、免疫紊乱、先天性酶缺乏、感染、环境因素、医源性因素(如化疗、放疗、盆腔手术)等多种因素有关。
目前是卵巢早衰的主要治疗选择,有助于改善围绝经期症状,降低骨质疏松和心血管疾病的风险,提高患者的生活质量。但是并不能从根本上恢复卵巢功能(比如激素分泌、卵泡生长或排卵)和生育能力。此外,激素替代疗法是否会增加乳腺癌风险尚不完全清楚。
冷冻的卵巢组织在患者条件允许时进行移植,有助于恢复一定的内分泌及排卵功能,使卵巢重新发生周期性变化。但卵巢组织冷冻保存后仍存在存活率低、自然受孕困难等诸多问题。
对于大多数有生育意愿的卵巢早衰患者,可通过捐赠的卵子,进行体外受精来实现怀孕的目的。不过捐赠的卵子供应是有限的,接受这些卵子的患者将无法生育和自己有血缘关系的孩子,同时,该方法也会涉及到社会伦理和法律问题,因而也有一定的局限性。
卵巢早衰其他治疗方法还包括补充孕激素、中药治疗、心理支持、饮食和运动调理、免疫调节等,但这些方法均无法从根本上改善卵巢功能,满足患者生育的需求。
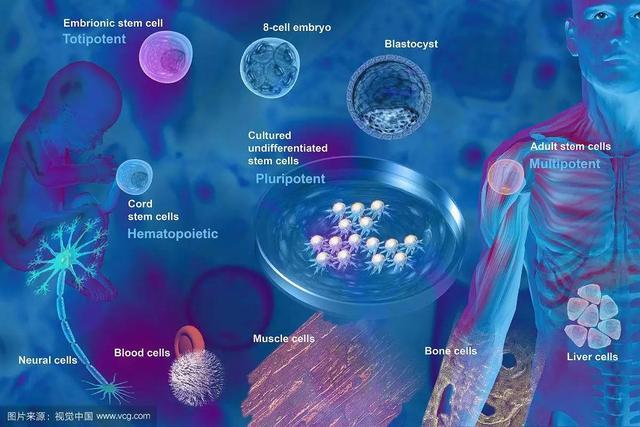
干细胞是是个体发育中的一类具有自我复制能力、多向分化潜能的非特异性细胞,具有自我更新和分化能力,可存在于早期胚胎中,还可以从胎盘、脐带、骨髓、血液、脂肪等诸多组织中分离出来,包括单能干细胞、多能干细胞(如间充质干细胞)、全能干细胞(如受精卵)等不同类型。
研究显示,通过干细胞治疗,可以刺激休眠卵泡,从而有助于在一定程度上逆转卵巢的衰老过程。研究人员可通过腹腔镜卵巢注射、经阴道超声(TVUS)引导下的卵巢注射、通过卵巢动脉输注(动脉内导管插入术)等方式,输注干细胞,以实现卵巢年轻化。

▲图源“摄图网”
间充质干细胞是一种起源于早期中胚层的多能干细胞,具有自我更新和多谱系分化能力,可以从骨髓、脐带、胎盘、脂肪组织和子宫内膜等组织中提取。其中,骨髓是间充质干细胞是重要的来源。目前多项人体试验表明(详见表1),间充质干细胞(MSC)可以促进卵泡发育,改善卵母细胞的质量、排卵和生育能力,而且它还具有归巢能力,输注人体后,可以迁移并附着在病变的卵巢上,并在多种激素和生长因子的作用下增殖,从而有助于恢复卵巢功能、治疗女性不孕症。
据环球网和遗传与发育生物学研究所的相关报道,中科院遗传与发育生物学研究所与南京鼓楼医院合作进行的干细胞复合支架材料治疗卵巢早衰的临床研究取得喜人的成果,作为受试者入组的方女士,于2018年在南京鼓楼医院成功诞下一名健康男婴,也标志着我国再生医学技术治疗卵巢早衰研究方面取得了较大的突破。下文会以骨髓和脐带来源的间充质干细胞为例,简单叙述一下干细胞如何对抗卵巢早衰。
表1 间充质干细胞治疗卵巢早衰的临床试验

(1)概述
具有来源丰富、免疫原性低、伦理考量少、自我更新和分化能力强等优点,在恢复卵巢功能和生育能力方面显示出巨大的潜力。研究表明,骨髓间充质干细胞可以通过多种机制(比如旁分泌、归巢、调节卵巢血管生成、抗纤维化、抗炎和免疫调节、抗氧化应激、抑制细胞凋亡、线粒体转移、自噬调节等),改善卵巢早衰患者的卵巢储备功能,以恢复卵巢激素的产生,重新激活卵泡发生,从而使卵巢储备功能较差的女性可以自然怀孕。
据2020年Igboeli P等人的相关文献显示,两位卵巢早衰的白人女性患者,在接受了自体骨髓间充质干细胞治疗后的7个月,卵巢雌激素的产生和月经来潮都得到了恢复。在治疗过程中,医生在患者髂嵴骨髓中,采集骨髓间充质干细胞,经过相应处理后,注射入患者右侧卵巢。之后对患者进行了1年的随访,在此期间,两名患者均出现过一次月经,而且更年期症状明显改善,血清雌激素水平较术前增加约150%。目前该试点临床研究已在ClinicalTrials.gov注册。如果您想了解骨髓间充质干细胞治疗卵巢早衰的更多信息,可以咨询国际干细胞研究医学部。
(2)骨髓间充质干细胞为什么能治疗卵巢早衰?
①旁分泌作用:
骨髓间充质干细胞可以合成和分泌多种趋化因子、生长因子和激素,包括血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)等,这些分子在血管生成、抗纤维化、抗炎和免疫调节、抗凋亡等方面发挥重要作用,从而改善局部微环境,促进受损组织的恢复。
研究表明,骨髓间充质干细胞可能会通过旁分泌作用,促进卵巢结构和功能的恢复。其中,脑源性神经营养因子可以促进卵母细胞成熟、促进胚胎发育;碱性成纤维细胞生长因子(bFGF)和血管内皮生长因子(VEGF)参与卵巢血管生成,有助于为颗粒细胞(GC)提供营养;同时,VEGF及其受体在抑制GC细胞凋亡、促进卵泡发育等方面发挥着重要作用。
②血管生成:
研究显示,间充质干细胞具有分化为内皮细胞、血管平滑肌细胞和其他类型细胞的潜力;该细胞还可分泌多种促进血管生成的生物活性因子,从而参与血管生成,而血管生成在修复受损卵巢方面发挥着重要作用。
相较于其他来源的间充质干细胞,骨髓间充质干细胞具有更高的血管生成活性,可以分化为内皮细胞、周细胞和血管壁,进而促进血管生成,有助于更好地修复卵巢损伤。
③抗炎和免疫调节作用
卵巢早衰患者卵泡中趋化因子和细胞因子水平异常升高,会通过细胞和旁分泌相互作用,诱发卵泡微环境的细胞内炎症,从而对卵母细胞质量、卵泡膜细胞的功能产生不良影响;还可吸引大量白细胞迁移到卵巢或激活大量免疫细胞,导致慢性低度炎症状态,从而进一步加剧卵泡闭锁和细胞凋亡,最终影响卵母细胞数量、卵泡质量。
来自炎症部位的信号分子,可促进骨髓间充质干细胞归巢,有助于抑制淋巴细胞增殖、炎症细胞因子产生,从而抑制局部炎症。
间充质干细胞的免疫调节功能主要是通过旁分泌活性、细胞间接触,以及与B细胞、T细胞、巨噬细胞、单核细胞、中性粒细胞等的相互作用来完成。此外,骨髓间充质干细胞分泌多种免疫调节介质,如前列腺素E2、转化生长因子-β(TGF-β)、肝细胞生长因子(HGF)等,在抗炎和免疫调节中发挥重要作用。
④抗纤维化作用
慢性炎症是驱动纤维化过程的主要因素之一,可以改变组织的正常结构并导致功能恶化,骨髓间充质干细胞表现出显着的抗炎生物活性,这可能是抑制卵巢纤维化的机制之一。
⑤抗凋亡作用
骨髓间充质干细胞可以通过调节B淋巴细胞瘤-2基因(bcl-2)、人体抑癌基因(p53)等凋亡相关基因的水平,抑制卵巢细胞的凋亡。此外,该细胞还可通话调节细胞周期蛋白D2(cyclin D2)和p21的表达,促进残余卵巢细胞的增殖,从而修复受损卵巢的结构和功能。
从人脐带中提取的间充质干细胞是脐带组织来源的干细胞,不仅保留了间充质干细胞的基本特征,而且具有较强的增殖和分化能力。研究显示,人脐带间充质干细胞可通过旁分泌途径,恢复卵巢功能;还可促进颗粒细胞增殖以及卵泡的产生和发育,从而快速修复卵巢损伤,还能治疗化疗引起的卵巢受损。
根据文献报道,有4例患者接受了卵巢内人脐带间充质干细胞注射治疗,并配合体外受精和胚胎移植治疗后,成功受孕且后代发育正常。
卵巢作为女性生理衰老的起搏器,往往比其他身体器官更早衰老,这又会反过来引发全身衰老,卵巢早衰不仅影响女性的容貌和身心健康,还会影响生育能力,很多女性也会因此而失去做妈妈的权利。而随着干细胞研究的不断深入,有望为卵巢早衰患者提供新的选择,在帮助女性维持青春的同时,也有助于女性重拾孕育的希望。不过该技术也存在一定的限制,比如免疫排斥、伦理问题等。如果您也想改善卵巢早衰问题,且想寻求干细胞这项新技术的帮助,可以咨询国际干细胞研究医学部,了解国内外临床应用的具体情况。
[1]Huang Y,et al.Bone marrow mesenchymal stem cells in premature ovarian failure: Mechanisms and prospects. Front Immunol. 2022 Oct 27;13:997808. doi: 10.3389/fimmu.2022.997808. Erratum in: Front Immunol.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9646528/
[2]Umer A,et al.The Therapeutic Potential of Human Umbilical Cord Derived Mesenchymal Stem Cells for the Treatment of Premature Ovarian Failure. Stem Cell Rev Rep. 2023 Apr;19(3):651-666. doi: 10.1007/s12015-022-10493-y. Epub 2022 Dec 15.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10070285/
[3]Pellicer N,et al.Herraiz S. Ovarian rescue in women with premature ovarian insufficiency: facts and fiction. Reprod Biomed Online. 2023 Mar;46(3):543-565. doi: 10.1016/j.rbmo.2022.12.011. Epub 2022 Dec 20.
https://www.rbmojournal.com/article/S1472-6483(22)00861-6/fulltext
[4]Igboeli P,et al.Intraovarian injection of autologous human mesenchymal stem cells increases estrogen production and reduces menopausal symptoms in women with premature ovarian failure: two case reports and a review of the literature. J Med Case Rep. 2020 Jul 18;14(1):108. doi: 10.1186/s13256-020-02426-5.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7368722/
[5]https://tech.sina.com.cn/roll/2018-01-29/doc-ifyqyqni
4605777.shtml
[6]https://sichuan.scol.com.cn/amsc/201605/54530079.html
1. 添加医学顾问微信,扫描☟二维码
2. 备注【您想咨询的问题】

我们致力于干细胞科普知识的推广与普及,专注于干细胞最新资讯提供和干细胞治疗专家咨询服务。
免责声明:本站内容仅供参考,不作为诊断及医疗依据