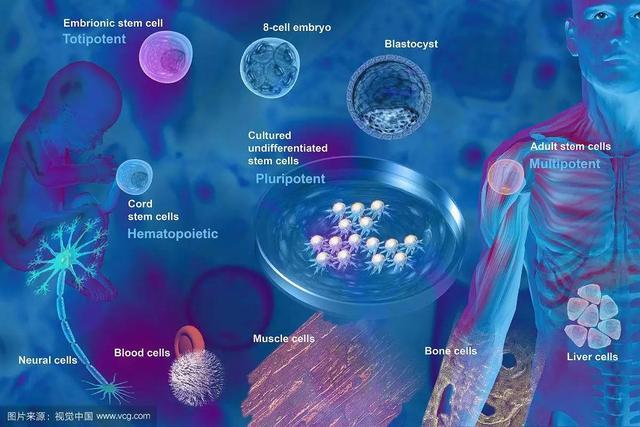
干细胞被认为是一种新的药物类别,展现出在现有药物中并未见到的独特功效,有望实现美容抗衰、某些难治性疾病防治的美好愿景。目前用于科学研究的人类干细胞主要有三类,即胚胎干细胞(ESCs)、成体干细胞(SSCs)、诱导多能干细胞(iPSCs)。其中临床研究和应用较多的是成体干细胞中的间充质干细胞。日本作为少数将干细胞获批应用的国家之一,遵循再生医学三级风险等级划分制度,目前获批应用的主要为自体干细胞,而非异体干细胞。
日本将与细胞治疗相关的研究和开发,称为“再生医学”。再生医学起源于胚胎学中的干细胞生物学,其治疗理念是通过干细胞,恢复受损组织及器官的功能。日本的再生医学监管一直由政府主导,日本将在医疗机构执行的干细胞临床研究和应用,认定为医疗技术,由厚生劳动省按照《再生医学安全法》进行监管。并根据细胞来源、处理方式、适用范围等风险等级不同,将再生医疗划分为以下三类:

▲图源“摄图网”
风险程度高于二三类再生医疗,常见包括同种异体干细胞、诱导多能干细胞(iPS细胞)、胚胎干细胞(ES细胞)、转基因细胞等。
除一类之外,大部分干细胞疗法和非同源细胞疗法均属于第二类再生医学,比如自体干细胞等。
用于疾病治疗的,除一、二类风险外的细胞疗法,常见包括树突状细胞(DC细胞)、自然杀伤细胞(NK细胞)、T细胞等。如果您还想了解再生医学的更多内容,可以咨询国际干细胞研究医学部。
日本干细胞在保证安全的基础上,建立了以促进临床研究、激发产业动能为目标的监管制度。第一、二、三类再生医疗技术均需向厚生劳动省提交研究或治疗计划,由厚生劳动省开展风险审查和备案,具体监管流程如下:
对于一类产品,除了常规提交、再生医学委员会的评估等步骤外,厚生劳动省还需在90天内,咨询健康科学委员会,并根据健康委员会意见做出最终决策。第一类再生医疗技术的具体审查流程见下图:

第二类再生医疗技术的具体审查流程详见下图:

第三类再生医疗技术的具体审查流程详见下图:

日本将异体干细胞归纳为第一类再生医疗范畴,尚未实现临床普及。不过我国目前临床研究应用较多的是异体脐带间充质干细胞。
已实现临床应用,包括自体脂肪间充质干细胞、自体骨髓间充质干细胞、自体滑膜干细胞、自体经血干细胞、自体子宫内膜组织来源的间充质干细胞等类型,其中以自体脂肪间充质干细胞应用更加广泛。关于自体干细胞获批产品,国际干细胞研究医学部之前做过详细介绍,大家可阅读原文:全面汇总:日本获批干细胞类型及适应证,涵盖糖尿病、关节炎、抗衰等多领域
以各类免疫细胞为主,常见包括NK细胞、DC细胞等,主要用于癌症治疗。
干细胞产品作为一种前沿的高科技产品,代表着人类医药发展史上较为复杂且颠覆性的技术,具有广阔的医疗用途和发展前景。但同时也因其独特属性,给研发人员和监管部门带来了前所未有的挑战。国际干细胞小编希望随着各国研究的不断深入,未来会有更多的干细胞获批应用,以满足患者的不同需求。如果您也有美容抗衰、慢病防治或提升免疫力等需求,且想寻求日本干细胞的帮助,可以咨询国际干细胞研究医学部,以获取临床应用的更多讯息。
本文为“国际干细胞研究”原创,转载需授权
[1]LI Yu,et al.The Experience and Enlightenment of Cell Therapy Regulation Dual-track System in Japan[J].China Biotechnology,2020, 40(1-2):174-179.
https://manu60.magtech.com.cn/biotech/CN/10.13523/j.cb.1906020
[2]陈云等.韩国与日本干细胞药品审批,监管及对我国的启示[J].中国新药杂志,2018,27(3):6.
doi:CNKI:SUN:ZXYZ.0.2018-03-003.
[3]聂永星等.日本干细胞双轨制监管对中国的经验借鉴[J].云南大学学报:自然科学版,2020,42(S02):5.
[4]https://saiseiiryo.mhlw.go.jp/
1. 添加医学顾问微信,扫描☟二维码
2. 备注【您想咨询的问题】

我们致力于干细胞科普知识的推广与普及,专注于干细胞最新资讯提供和干细胞治疗专家咨询服务。
免责声明:本站内容仅供参考,不作为诊断及医疗依据